ホメオスタシス(恒常性)とは身体機能の安定を示すが、それは静的なものではなく、動的環境の中で常にバランスを取っているものである。

アーロン・フィリップス准教授
写真:ライリー・ブラント(カルガリー大学)
脳と体の間では、脊髄や脳神経を介して絶え間なく情報が行き来し、変動を感知して自律神経系を調整しています。脊髄損傷が起こると、このフィードバック機構が変化あるいは断絶し、恒常性の維持が危険なほど乱れることがあります。
脊髄損傷により発症する自律神経過反射(Autonomic dysreflexia) は、脊髄損傷後に生じた新たな神経回路で血圧が調整される状態を示します。本来は「感覚」として認識される刺激が、極端な高血圧発作を引き起こすようになり、症状は発汗のような軽度のものから、脳卒中・けいれん・心停止といった重篤なものまで及びます。脊髄損傷を抱える人々にとって、この生命を脅かす事態はいつでも起こり得るのです。
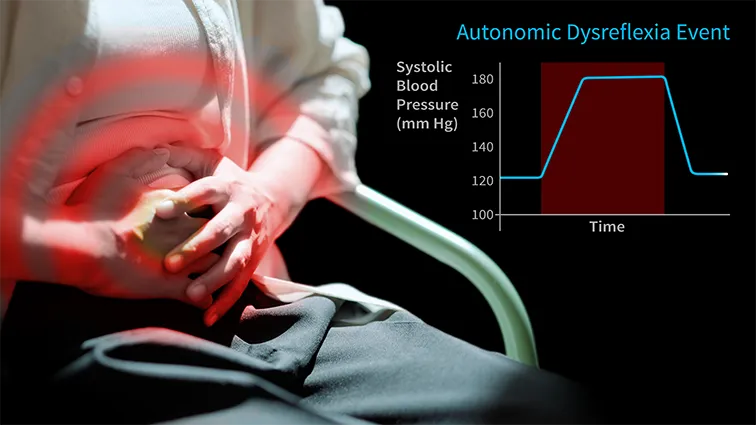
下腹部の圧迫、損傷、感染症が自律神経過反射の引き金になることがある。
Nature と Nature Medicine へ掲載された関連論文において、アーロン・フィリップス教授と彼のチームは、自律神経過反射の基盤となる神経構造と、それを治療するために開発した電気刺激プロトコルについて報告しています。これらの論文は、同チームが脊髄損傷後の不安定な血圧を確実に安定化させる硬膜外刺激装置「神経補綴的バロレフレックス(neuroprosthetic baroreflex)」を発表してから、わずか4年後の成果です。今回の新しい発表では、神経補綴的バロレフレックスで基盤を築いた研究をさらに発展させ、その装置が標的とした「血行動態ホットスポット」をより正確に調べ、その知見を用いて硬膜外電気刺激を治療法として精密に調整しています。
関連リンク: 血行動態の不安定性 ― 見えない問題の解決
この2つの論文には、高度なスキルと正確な実験が詰め込まれており、動物モデルによる自律神経過反射の再現から、実際にこの病態を抱えるヒト被験者へ刺激装置を埋め込んで試験するまで、チームが踏んだ科学的旅路のすべてが詳細に記されています。この研究においてアーロン教授らは、科学においてはほとんど不可能と思われる偉業を成し遂げています。すなわち、「問題を完全に理解し、そしてそれを解決する」ことです。本ブログでは、この2つの論文のうち最初のものを取り上げますが、両方読むことを強くお勧めします。
Nature: A neuronal architecture underlying autonomic dysreflexia
Nature Medicine: An implantable system to restore hemodynamic stability after spinal cord injury
左からRobyn Cameron、Kelly Larkin-Kaiser、Catherine Veilleux、Robin Demesmaeker、Fady Girgis、Kyle Rogan、Aaron Phillips、Nico Hankov。
自律神経反射異常のモデル化
研究チームは、まず自律神経過反射の信頼できる臨床モデルを開発することから始めました。ヒトでは、この病態は脊髄損傷後に発生します。主に下腹部における持続的な圧迫や損傷(例:膀胱や腸の拡張、褥瘡、感染など)が引き金となる傾向があります。
マウスモデルでは、脊髄のT4レベルで切断を行い、さらに直腸結腸領域を機械的に拡張させることで作製しました。自律神経過反射は、脊髄損傷から約2週間後に始まり、4週間後にピークを迎えました。この発症の遅れは、その原因が損傷後の脊髄神経の再編成に関連している可能性を示唆しています。
原因となるニューロンの特定
動物モデルを用いることで、チームは自律神経過反射によって引き起こされる脊髄の変化を安定して追跡することができました。彼らは脊髄を透明化し、標識を付け、画像化し、さらに神経興奮マーカーであるFosの発現量を測定しました。Fosの発現量が多い部位では、自律神経過反射に応答した遺伝子発現がより多いため、神経の再編成に関わる「犯人」である可能性が高いと考えられました。その結果、2つのホットスポットが特定されました:L5-S1セグメントおよびT11-T13セグメントです。
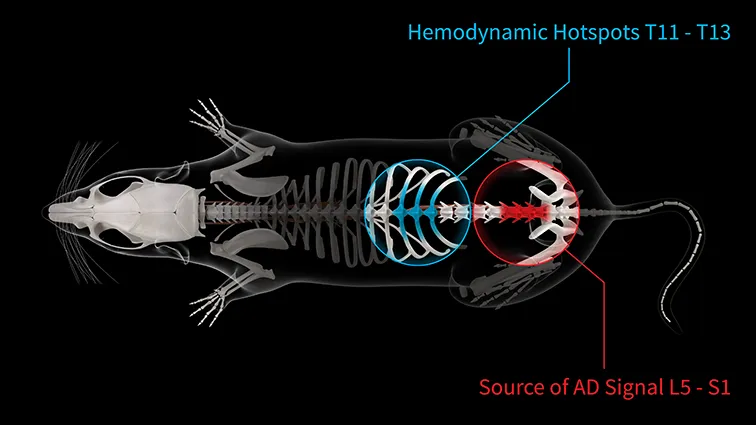
脊髄分節L5-S1とT11-T13は、自律神経反射異常の後、遺伝子発現マーカーFosの量が最も多かった。
チームは、これらの神経が発現する神経伝達物質や、さまざまな分子に対する反応を特定し、単一核RNAシーケンシング(single-nucleus RNA sequencing)によってそれらを複数のサブカテゴリーに分類しました。さらに、独自に開発した「Augur」と呼ばれる機械学習手法を用いて解析を行い、自律神経過反射の際に最も反応性の高いニューロンを分離することに成功しました。
脊髄損傷前、腰仙部のホットスポット内のニューロンは、到達動作や歩行などの運動行動に関与しており、血圧調節とはまったく関係がありませんでした。ところが損傷後、これらのニューロンは胸椎部ホットスポットへと長い投射を伸ばすようになっていました。この胸椎部ホットスポットは、過去の研究で血行動態を媒介する領域として同定されていたものです。
つまり、これまで運動制御に使われていた神経が再編成され、血行動態のホットスポットを刺激するようになったのです。重要なことに、L5–S1セグメントを刺激すると、自律神経過反射が時間とともに悪化することが確認されました。
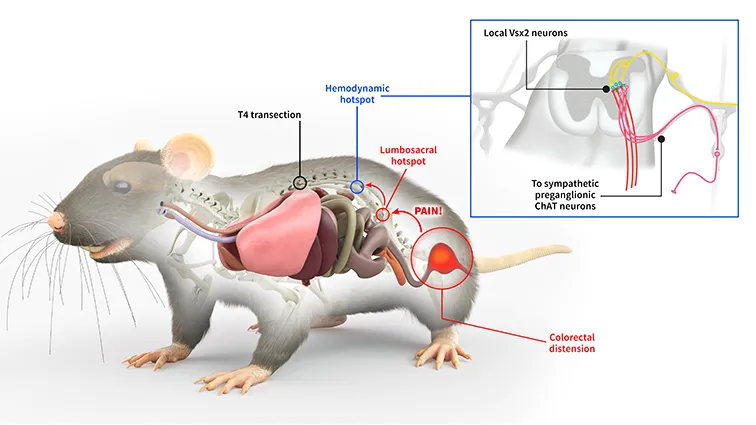
自律神経反射異常の全脊髄経路:侵害受容性出力は大腸脹満部位を離れ、腰仙部ホットスポットに移動し、長投射Vsx2ニューロンを介して血行動態ホットスポットに移動し、交感神経前接合ChATニューロンを介して血行動態に影響を与える。
治療法の開発
次にチームは、ニューロンのサブポピュレーション追跡を再び行いました。今回は、以前に血行動態の安定を回復させることが示されていた血行動態ホットスポットの刺激後に活性化されるニューロンに焦点を当てました。
その結果、硬膜外電気刺激(epidural electrical stimulation; EES)によって、固有感覚ニューロン(proprioceptive neurons)が動員され、自律神経過反射時と同じChATニューロンを活性化することがわかりました。
つまり、この領域への硬膜外電気刺激が自律神経過反射を上書きし、神経回路そのものをリハビリし、症状を消失させる可能性があることが示されたのです。
ただし、この方法は予測が難しく、危険を伴う可能性もありました。症状が適切に制御できるか、またこの治療がさらなる神経再編成を引き起こして自律神経過反射を再発・悪化させないかを確認するため、長期的なモニタリングが必要でした。
長期の安全性試験
安全性試験を行うためには、疾患モデル・治療法・長期連続血圧モニタリングの3つが必要でした。チームは既存の脊髄損傷ラットモデルを用いて自律神経過反射を誘発し、硬膜外電気刺激による治療を開始しました。
6週間にわたり、Kaha 交感神経・血圧送信機を使用してラットの血圧を連続的にモニタリングしました。自律神経過反射は進行性であり、突発的に悪化することもあるため、このような長期・連続モニタリングが特に重要でした。
6週間の経過中、チームは血圧制御の継続的な改善を確認し、最終的にシステムが安定化、自律神経過反射は完全に消失しました。
神経リハビリテーションは成功したのです。
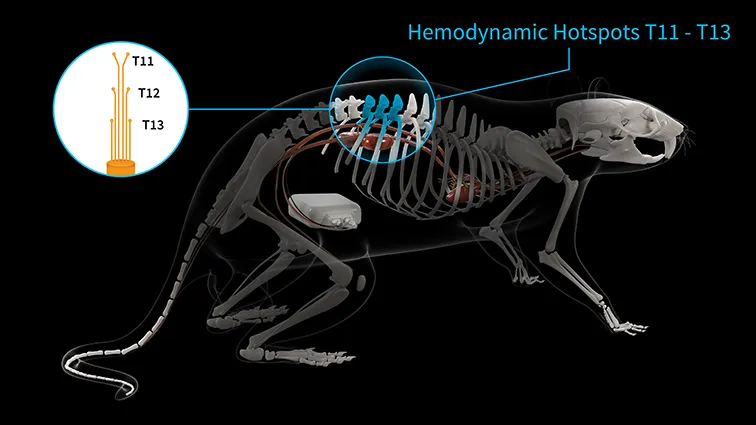
ラットの生体に埋め込まれた硬膜外電気刺激装置(EES)でT11-T13の血行動態ホットスポットが刺激された状態で、Kahaテレメーターが6週間にわたって連続血圧モニタリングを行った。
関連記事 無料ガイド: 神経生理学のためのKahaテレメトリー
ヒトへの応用
自律神経過反射は、四肢麻痺患者のおよそ80%に発生します。そのうち治療を受けている人でも90%以上が依然として症状を経験しています。
これらの症状は常に命に関わるものではないものの、生活の質を著しく低下させます。たとえば不安、頭痛、動悸、そして将来的な重篤な副作用への常時の恐れなどです。
研究室から臨床への移行は容易ではありませんが、このケースでは被験者にとって明確な利益が存在しました。
Nature Medicine誌に掲載された論文の中で、Aaron Phillips教授とチームは、カナダ、スイス、オランダでのヒト参加者による神経リハビリテーション手法の試験過程について詳述しています。
彼らはこの手法を最適化し、ONWARD Medical社との共同で臨床試験へと進む段階に入っています。
2022年8月、第1回HEMOトライアル・インプラント手術中のアーロン・フィリップス主任研究者(左)とケリー・ラーキン=カイザー共同研究者。
続きを読む
A neuronal architecture underlying autonomic dysreflexia | Nature
An implantable system to restore hemodynamic stability after spinal cord injury | Nature Medicine

アーロン・フィリップス博士
カルガリー大学准教授。神経系と心血管系の複雑な相互作用、特に臨床疾患に寄与する部分の解明へ情熱を抱き、アーロンの研究は神経関連の健康問題を抱える人々に向けた新規治療法の開発へ焦点を当てている。
